Servicios Personalizados
Articulo
Indicadores
Links relacionados
 Citado por SciELO
Citado por SciELO
 Similares en SciELO
Similares en SciELO
Bookmark
BIOFARBO
versión impresa ISSN 1813-5363
BIOFARBO v.17 n.2 La Paz 2009
TRABAJOS DE INVESTIGACIÓN
Diversidad y distribución de bacterias sulfato reductoras en sedimentos de lagunas de la cuenca Milluni contaminada por desechos mineros
Diversity and distribution of sulfate-reducing bacteria at Milluni lakes sediments contaminated with acid mine drainages
Sonia Sacaca C. 1, Volga Iñiguez R. 1, Marc Roulet 2
1 Universidad Mayor de San Andrés, Carrera de Biología, Instituto de Biología Molecular y Biotecnología
2Institut de Recherche pour le Développement
Dirección para correspondencia: Sonia Sacaca C. Instituto de Biología Molecular y Biotecnología, Carrera de Biología, Universidad Mayor de San Andrés. Campus Universitario, Cota Cota. La Paz, Bolivia.
E mail: isela11903@hotmail.com
Recibido para publicación en 21/08/09
Aceptado en 30/11/09
RESUMEN
Las bacterias sulfato reductoras (BSR) juegan un rol importante en la mitigación de los drenajes mineros ácidos, reduciendo el sulfato a sulfuro de hidrógeno que se combina con los metales pesados precipitándolos. De esta manera las BSR contribuyen a reducir tanto la acidez del medio como la concentración de metales pesados solubles, por lo que su estudio es importante, en ambientes contaminados por la minería.
La Cuenca Milluni, localizada al norte de la ciudad de La Paz, presenta altos niveles de contaminación por desechos mineros, como resultado de la explotación minera realizada desde el siglo pasado. En el presente estudio, mediante el uso de métodos moleculares en base al gen 16S DNAr y su amplificación mediante Nested-PCR, se evaluó la distribución de los subgrupos de BSR en perfiles sedimentarios de lagunas de la Cuenca y en muestras de turbera, donde se evidenció la presencia de BSR con distribución espacial definida, bajo diferentes condiciones físico-químicas de Eh (+350 a -330 mV) y pH (10 a 2.5). Se observó una considerable variación en la distribución de BSR donde los subgrupos Desulfovibrio-Desulfomicrobium (DSV-DMB) y Desulfococcus-Desulfonema-Desulfosarcina (DCC-DNM-DSS) fueron los más encontrados. La variación de las características físico-químicas y la ubicación de las lagunas con respecto a la mina, condicionarían la distribución y adaptación de las BSR en sistemas heterogéneos, proyectándolas como herramientas para procesos de bio-remediación de aguas contaminadas por drenajes mineros ácidos y metales pesados en la región.
Palabras Clave: bacterias sulfato reductoras (BSR), Drenaje Minero Acido (DMA), gen16S rRNA
ABSTRACT
The anaerobic sulphate-reducing bacteria (SRB) may play an important role in acid mine drainage mitigation, lowering sulphate concentrations derived from Acid Mine Drainage (AMD), by promoting metal sulphides precipitation and producing local alkalinity. The present study was carried out at the Milluni Lakes located in the Altiplano highlands north from La Paz city, to determine diversity and distribution of SRB. The Milluni region has accumulated mining waste as a result of unregulated heavy-metal mining since the past century. SRB subgroups distribution along a deep profile in sediments and wetlands samples contaminated with AMD of different physicochemical conditions was analyzed by PCR and nested-PCR of 16S DNAr. Results evidenced presence of SRB with defined spatial distribution in all analyzed lakes representing a wide range of physico-chemical conditions of Eh (+350 to -330 mV) and pH (10 to 2.5). Along the sediment profiles, considerable variation in SRB- distribution was evident, being Desulfovibrio-Desulfomicrobium (DSV-DMB) and Desulfococcus-Desulfonema-Desulfosarcina (DCC-DNM-DSS) the most commonly found subgroups. The variable physico-chemical conditions and lakes location to the mine may have conditioned distribution and adaptation of SRB projecting them as a potential tool for bioremediation in this region.
Key Words: Sulphate-reducing bacteria (SRB); Acid mine drainage (AMD); 16S rRNA gene
INTRODUCCIÓN
La contaminación de suelos y cuerpos de agua es un problema ambiental común en Bolivia, por lo que es importante el estudio de comunidades bacterianas con potencial de bioremediación. Bolivia se caracteriza por una larga tradición en la explotación de minerales desde la época colonial, bajo un inadecuado o casi inexistente control ambiental.
En la región del valle de Milluni rica en depósitos de sulfito, a más de 4000 metros sobre el nivel del mar (m.s.n.m.) en la Cordillera Real de los Andes, al norte de la ciudad de La Paz se encuentra la mina La Fabulosa donde se explotan desde hace más de 50 años minerales como el estaño, zinc y plomo. En esta región se encuentra la cuenca de Milluni, comprendida por: lagunas Pata Khota (PK), Jankho Khota (JK), Ventanani (V), laguna residual Milluni Chico (MCH) y el lago Milluni Grande (MG). Estas dos últimas están próximas a la mina y reciben directamente los efluentes de drenajes mineros ácidos (DMA) provenientes tanto de la mina como del inadecuado depósito de las colas de desmonte, que contienen sulfuros metálicos asociados a la pirita (FeS2) que al oxidarse generan valores de pH bajos y elevada concentración de metales pesados disueltos (Pb, Cu, Zn, Sn, Fe, Cd, As, Sb, Co)1. Las elevadas concentraciones de metales pesados han provocado un deterioro del medio ambiente en la región, afectando al ecosistema acuático y terrestre, poniendo en riesgo la flora y fauna local así como a las comunidades aledañas2.
Dentro los desechos mineros existe una diversidad de bacterias, entre las que destacan por su potencial de biorremediación, las Bacterias Sulfato Reductoras (BSR). Las BSR reducen el sulfato (SO4-2) en condiciones anaerobias hasta H2S, el cual luego se combina con los metales pesados, precipitando a los mismos como sales de sulfuro3, 4, 5, 6.
De esta manera las BSR cumplen en estos ambientes dos funciones importantes; por un lado reducen la acidez de las aguas mediante la formación de bicarbonato por la oxidación de compuestos orgánicos y por otro precipitan los metales pesados disueltos7, 8.
Debido a dificultades en su cultivo, las BSR son más accesibles a ser identificadas por métodos moleculares, mediante el análisis de los ácidos nucleicos, empleando marcadores, como el 16S DNAr9, 10. El presente trabajo tiene por objeto analizar en muestras de perfiles sedimentarios, de cuerpos de agua de la cuenca minera de Milluni, la distribución de subgrupos de BSR asociada a diferentes grados de contaminación por desechos mineros y dentro de condiciones físico-químicas variables (Eh, pH).
MATERIAL Y MÉTODOS
Área de estudio. La Cuenca Milluni se encuentra en las faldas del glaciar del Huayna Potosí, entre 4500 y 4700 m.s.n.m., a 30 Km. de la ciudad de La Paz con una ubicación entre 16º08` a 16º10` latitud sur y de 68º17` a 68º 21` longitud oeste.
En el estudio se incluyeron (Figura 1) a las lagunas Pata Khota (PK) y Jankho Khota (JK) ubicadas en la zona alta de la cuenca que presentaron vegetación acuática. A la laguna Ventanani (VN) ubicada al Este de la cuenca dentro de una zona que contiene óxidos de hierro precipitados y ausencia de vegetación.
|
Lagunas de estudio: PK = laguna Pata Khota, JK = laguna Jankho Khota, VN= laguna Ventanani, MC= Desecho minero Milluni Chico, MG= laguna Milluni Grande y TM = Turbera Milluni. Figura 1. Mapa Cuenca Milluni (Coadaptado de Salvarredy-Aranguren et al., 2008) |
La laguna residual Milluni Chico (MC) y el lago Milluni Grande (MG), situados corriente abajo en la zona colindante y directamente afectadas por la mina, en donde no se observó vegetación.
Finalmente, a la salida de la cuenca, la turbera Milluni (TM) que presenta restos de vegetación en descomposición, formando una gruesa capa de suelo orgánico y constituye un sitio de retención de aguas contaminadas.
Colecta de las muestras. La colecta de muestras y las mediciones ambientales se realizaron en época seca en el mes de Agosto del 2003, cada punto de muestreo (cm.) fue tomado manualmente con un saca testigos de 1.20 m., equipado con tubos de policarbonato. La manipulación de las muestras fue realizada con material de plástico, previamente lavado con ácido clorhídrico al 10%, agua Milli-Q e irradiado con luz UV. Las muestras fueron refrigeradas a -20°C hasta el momento de su procesamiento.
Mediciones físico-químicas (Eh y pH). El potencial de oxido-reducción (Eh) fue medido in situ a intervalos de 1 cm., mediante microsondas de platino con un electrodo de referencia (Ag/AgCl2) y un Eh-metro Consort, calibrado con una solución patrón de + 220 mV.
Para el pH se utilizó un pH–metro calibrado con soluciones estándar (pH 4, pH 7 y pH 10), las muestras luego fueron colectadas en tubos de plástico cónicos y estériles.
Extracción de DNA de muestras de sedimentos. Muestras de sedimento, 500mg., fueron mezclados en tubos de 1.5 ml, con 810 µl de solución de lisis (100mm Tris-HCl (pH 8.0), 100 mM Na2EDTA (pH 8.0), 100 mM de fosfato de sodio (pH 8.0), 1.5 mM de NaCl y 2% de bromuro hexadecil-trimetil amonio (CTAB)) y 6 µL de proteinaza K (10 mg/ml). La mezcla fue agitada en forma horizontal a 225 rpm por 40 min., adicionando después 1800 µL de SDS al 10% con posterior incubación a 65ºC por 2 horas con suaves inversiones cada 15 minutos. Posteriormente los tubos fueron centrifugados a 6000 rpm por 10 min., recuperándose el sobrenadante (aprox. 600 µL). Al precipitado residual se agregaron 408 µl de solución de lisis y 60 µl de SDS (10%), incubándose la mezcla a 65 ºC por 10 min., se recuperó el sobrenadante por centrifugación. Ambos sobrenadantes fueron mezclados con cloroformo-alcohol isoamílico, seguidos de una centrifugación a máxima velocidad (14000 rpm) por 5 minutos. Se adicionó al sobrenadante isopropanol (0.8 volúmenes) y acetato de sodio (0.3 M) dejándolo reposar verticalmente por 1 hora. Posteriormente la mezcla fue centrifugada a una máxima velocidad por 20 minutos, desechándose por inversión el sobrenadante. Al precipitado se le agregó etanol al 70%, con una posterior centrifugación a máxima velocidad por 10 min. El precipitado obtenido fue disuelto en agua destilada a 4 ºC por 15 horas11. La detección del DNA total se efectuó por electroforesis con solución tampón TBE 0.5X en geles de agarosa al 1% en presencia de bromuro de etidio, la visualización del DNA se realizó en un transiluminador de luz UV.
Purificación del DNA de sedimentos. Se empleó el Kit comercial de extracción y purificación UltraClean Soil DNA (MoBio Inc.) y columnas elaboradas con Sefarosa. El DNA purificado fue evaluado por electroforesis en geles de agarosa al 1% con 0.5 μg/ml de bromuro de etidio con solución tampón TBE 0.5X y visualizado en un transiluminador de luz UV.
Amplificación del 16S DNAr y subgrupos específicos de BSR por PCR y Nested-PCR.
Los cebadores utilizados en la amplificación por PCR del gen 16S DNAr fueron FD1 (AGAGTTTGATCCTGGCTCAG) y RP2 (ACGGCTACCTTGTTACGACTT). La amplificación fue realizada en un termociclador (modelo TD 7500, Hybaid, USA), bajo el siguiente programa: 1 ciclo inicial a 95 ºC por 1 min., 30 ciclos de 94 ºC por 1 min., 50-65 ºC por 1 min., y 72 ºC por 1 min., con una extensión final a 72 ºC por 5 min., los componentes del Master Mix fueron: 1.7 µl de agua, 2 µl de tampón PCR 10X (Promega), 2 µl de MgCl2 10X, 2 µl de cebador (5 pmol/µl), 0.4 µl dNTPs (10 mM), 0.5 µl (10 µg/µl) de BSA, 0.05 U/µl (DNAr 16S) y 0.02 U/µl de Taq Polimerasa (Promega), finalmente DNA (2-20 ng). Los productos se analizaron por electroforesis con TBE 0.5X en geles de agarosa 0.8%-1.5% en presencia de bromuro de etidio y posterior visualización. El producto de la amplificación del gen 16S DNAr fue de 1504 pb.
Se realizó Nested-PCR para la identificación de los sub-grupos de BSR se utilizaron cebadores específicos para cada sub-grupo de BSRs:
Sub-grupo 1 Desulfotomaculum (DFM) (TAGMCYGGGATAACRSYKG, ATACCCSCWWCWCCTAGCAC).
Sub-grupo 2 Desulfobulbus (DBB) (CGCGTAGATAACCTGTCYTCATG, GTAGKACGTGTGTAGCCCTGGTC).
Sub-grupo 3 Desulfobacterium (DBM) (CTAATRCCGGATRAAGTCAG, ATTCTCARGATGTCAAGTCTG).
Sub-grupo 4 Desulfobacter (DSB) (GATAATCTGCCTTCAAGCCTGG, CYYYYYGCRRAGTCGSTGCCCT).
Sub-grupo 5 Desulfococcus-Desulfonema-Desulfosarcina (DCC-DNM-DSS) (GATCAGCCACACTGGRACTGACA, GGGGCAGTATCTTYAGAGTYC).
Sub-grupo 6 Desulfovibrio-Desulfomicrobium (DSV-DMB) (GRGYCYGCGTYYCATTAGC, SYCCGRCAYCTAGYRTYCATC)9.
RESULTADOS
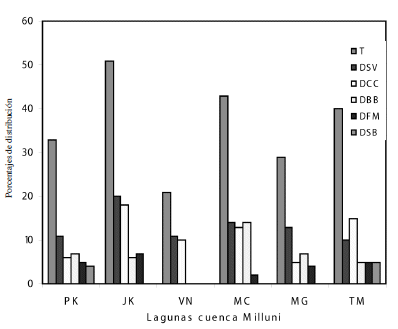
Distribución de subgrupos de BSR en perfiles sedimentarios de cuerpos de agua de la Cuenca Milluni. La distribución de BSR en lagunas situadas por encima de los 4600 m.s.n.m. (cuenca arriba) alcanzó un 51% en Jankho Khota seguida de Pata Khota (33%), en contraste con Ventanani donde el porcentaje fue menor (21%) y donde se observó la menor diversidad de subgrupos de BSR en toda la cuenca (Figura 2). En la región colindante a la mina ubicada entre los 4400 m.s.n.m. (cuenca abajo), con influencia directa por los desechos mineros, se observaron valores entre 29% Milluni Grande y 43% Milluni Chico bajo condiciones de pH ácido. Así mismo, dentro la Turbera Milluni se observó una distribución de BSR del 40% (Figura 2).
|
Pata Khota (PK); Jankho Khota (JK); Ventanani (VN); Milluni Chico (MC); Milluni Grande (MG); Turbera Milluni (TM), T= Total distribución de BSR; DSV = Desulfovibrio; DCC = Desulfococcus; DBB = Desulfobulbus; DFM = Desulfotomaculum; DSB =Desulfobacter. Figura 2. Distribución de sub-grupos de Bacterias Sulfato Reductoras en lagunas y turbera de la cuenca Milluni |
En relación a la diversidad encontrada de los subgrupos de BSR; DSV-DMB y DCC-DNM-DSS fueron los más predominantes en todas las lagunas, tanto bajo condiciones de Eh oxidante y reductor como pH ácido y alcalino, en contraste a los subgrupos DBB y DFM que si bien fueron identificados en sedimentos con Eh variable y pH ácido (MC y MG), no fueron encontrados en ambientes altamente oxidantes (laguna VN).
Asimismo, el subgrupo DSB se restringió a sedimentos que presentaron mayor cobertura vegetal (PK y TM) (Figura 2). El subgrupo DBM no fue encontrada en ninguna de las muestras analizadas.
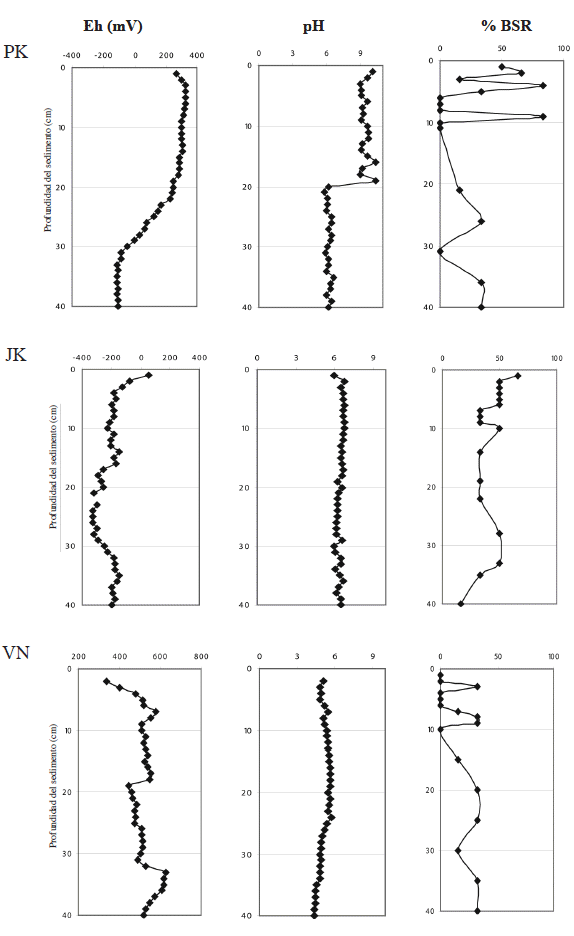
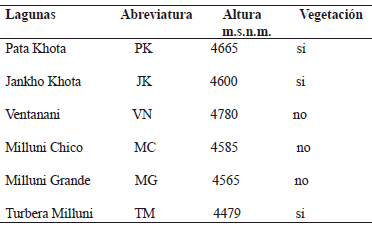
Cuenca arriba de la mina. PK ubicada en una zona granítica no mineralizada, presentó un sedimento de estructura arcillosa y color marrón (tabla 1). A nivel de la superficie (1 a 19 cm.), el Eh fue oxidante (+370 a +31 mV) y el pH alcalino (9-10), con transición en la parte profunda del sedimento a un Eh reductor con valores entre -6 a -118mV, en concordancia con los cambios en el pH hacia valores mas ácidos (pH 5-6) (Figura 3 PK).
La distribución de BSR a lo largo del sedimento fue mayor en los primeros 10 cm. alcanzando hasta un 83% y fue disminuyendo a mayor profundidad hasta un 33% (40 cm.) (Figura 3 PK).
|
Figura 3. Factores físico-químicos (Eh y pH) y distribución de Bacterias Sulfato Reductoras en lagunas Pata Khota, Jankho Khota y Ventanani. Eh = potencial de oxido-reducción, pH y % = Porcentaje de distribución de BSR. |
JK ubicada en la cuenca media, presentó un sedimento de estructura arcillosa y de color café-gris (tabla 1). El Eh ligeramente oxidante en la superficie (hasta los 2 cm.) (+51 a -331 mV), cambiando luego a un Eh reductor. Los valores de pH presentaron características ligeramente ácidas entre 6 a 6.7 (Figura 3 JK).
La distribución de BSR se observó a nivel de todo el perfil sedimentario predominando en los primeros 10cm. (66%) y disminuyendo (hasta16%) en la parte profunda (40 cm.) (Figura 3 JK).
VN ubicada dentro de una zona mineralizada sin influencia directa de la mina, presentó un sedimento constituido por arena y grava de color marrón claro (Tabla 1). Se observaron valores de Eh oxidante entre +292 a +629 mV a nivel de todo el perfil sedimentario. El pH presentó valores entre 5.7 a 4.24, más ácidos que en PK y JK (Figura 3 VN). En VN la distribución de BSR fue menor en la superficie (16%) incrementando a mayor profundidad del sedimento (33%) (Figura 3 VN).
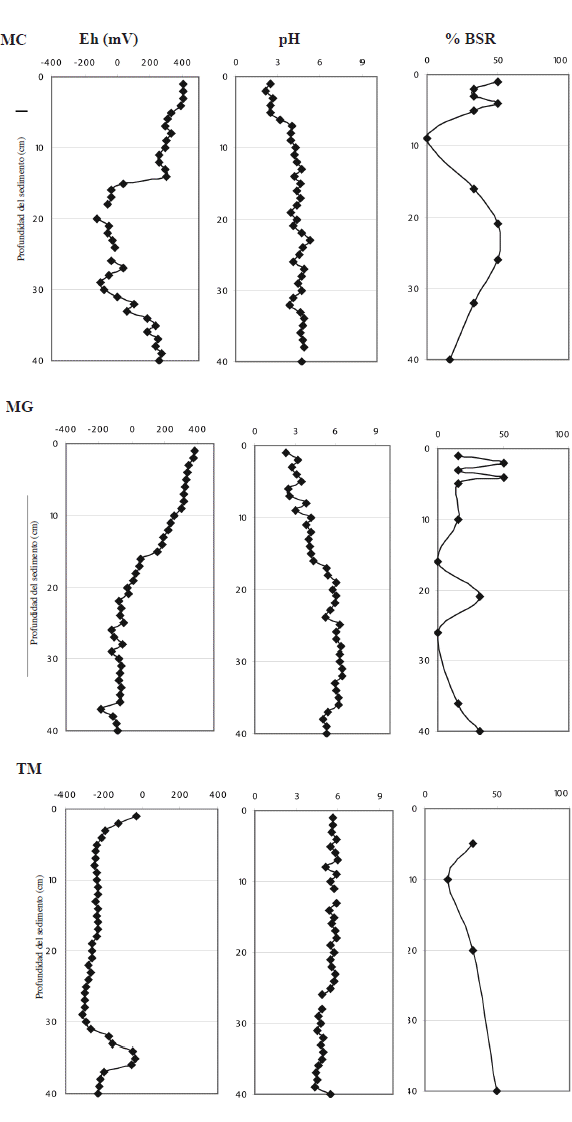
Cuenca abajo de la mina. MC, donde se acumulan residuos de colas de desmonte, presentó un sedimento con estructura arcillo-arenoso y de color gris oscuro. El Eh oxidante tanto a nivel de la superficie (+250 a +400 mV.) en los primeros 15 cm. como en la profundidad (+100 a + 260 mV) entre los 30 a 40 cm., presentó una zona de transición a Eh reductor en la parte central del sedimento. El pH mostró valores más ácidos (pH 2.1) en la superficie que en la profundidad (pH 4.9) (Figura 4 MC). La distribución de BSR en MC, fue mayor en la superficie y en la parte central del sedimento (50%) (entre 1 a 26 cm.), disminuyendo hasta un 16% con la profundidad (40cm.) (Figura 4 MC).
| Figura 4. Factores físico-químicos (Eh y pH) y distribución de Bacterias Sulfato Reductoras en lagunas Milluni Chico, Milluni Grande y turbera Milluni. Eh = potencial de oxido-reducción, pH y % = Porcentaje de distribución de BSR |
MG ubicada en la parte baja de la cuenca, representa una zona de sedimentación natural de los desechos provenientes de MC. En esta región en el sedimento se encontró arcilla, limo y arena de color ocre (Tabla 1). En los primeros 10 cm. se observo un Eh oxidante así como un pH acido entre 2.5 -5. En la parte profunda un Eh reductor (+383 a -190 mV) (Figura 4 MG) y pH más cercano a la neutralidad (6). La distribución de BSR en MG fue mayor en la superficie (entre 1 a 5cm.) alcanzando un 50% y luego fue disminuyendo (33%) con la profundidad (Figura 4 MG).
TM presentó un sedimento constituido por materia vegetal, de color verde marrón (Tabla 1). La turbera presento un Eh reductor (-29 a -310 mV), estable entre los 5 – 30 cm. con cambios en la parte profunda (40cm.). El pH osciló entre 5.6 a 4.4 y se mantuvo relativamente constante a lo largo de todo el perfil sedimentario (Figura 4 TM).
La distribución de BSR se caracterizó por un incremento (33%-50%) en la profundidad del sedimento (Figura 4 TM).
DISCUSIÓN
Los resultados de este trabajo muestran la presencia de diversos subgrupos de BSR en perfiles sedimentarios de cuerpos de agua ubicados a gran altura, (por arriba de los 4500 m.s.n.m.), en la región minera de Milluni en el altiplano boliviano caracterizada por condiciones climáticas de stress, con rangos de temperatura anuales entre -6 ºC y 17 ºC y alta radiación solar. Un total de cinco de los seis subgrupos de BSR fue observado bajo diversas condiciones de Eh oxidante-reductor y pH ácido-alcalino. Así, se abre la posibilidad de explorar en el futuro la actividad metabólica de las BSR, asociada a la precipitación de metales pesados.
En otros estudios se ha identificado a BSR en diversos ambientes incluidos los DMA por métodos dependientes de cultivo3,12,13. Así, mediante análisis de ácidos grasos se encontró a los subgrupos DSV y DBB en ambientes ácidos y en presencia de óxidos de hierro. Son pocos los estudios que han enfocado la composición de subgrupos de BSR por métodos moleculares. Se ha reportado14 la presencia de miembros del grupo delta Proteobacteria en AMD de China usando librerías de 16SRNA. Varios estudios se enfocan en el subgrupo DFM -Desulfosporisinus como el mas relevante en ambientes extremos15, 16 y de utilidad en bioremediación17.
La distribución espacial encontrada de subgrupos de BSR estaría influenciada por adaptaciones fisiológicas a las condiciones de cada sitio. Sin embargo es importante considerar las limitaciones inherentes al método de detección que no permite una estimación cuantitativa del número de BSR, no refleja directamente la actividad metabólica y puede estar sesgado por la cobertura de los primers utilizados para la identificación de los subgrupos de BSR. Por lo que futuros estudios deberán evaluar la diversidad de BSR mediante métodos más específicos como la secuenciación.
Lagunas Pata Khota y Jankho Khota. En la cuenca arriba, las lagunas naturales PK y JK se encontraron menos afectadas por la contaminación directa de la mina La Fabulosa. Esto puede observarse a través de los valores de pH alcalino-neutrales a lo largo del sedimento, que estarían asociados tanto a las mayores concentraciones de HCO3- y Ca2+ como a las menores concentraciones de SO-24 1.
El Eh oxidante de la laguna PK en los primeros centímetros (28 cm.) de profundidad, podría estar influenciado por la presencia de plantas acuáticas cuyas raíces perturbarían el sedimento a este nivel. En este estrato el pH alcalino estaría asociado a la baja concentración de SO-24 (la menor de la cuenca) y a la influencia de las aguas del glaciar Huayna Potosí que presentarían una mayor concentración de HCO3- debido a la disminución de la precipitación fluvial durante la época de muestreo.
La diversidad de subgrupos de BSR encontrada en los 15 cm., donde se observan 5 de los 6 subgrupos analizados podría estar influenciada por los exudados de las raíces de plantas acuáticas que contribuirían al desarrollo de las BSR y otras comunidades bacterianas. Así mismo, de estar presente, la actividad metabólica de las BSR en los primeros centímetros de profundidad (10 cm.) podría contribuir a la producción de HCO3- que también favorecería a los valores de alcalinidad observados.
En este entorno, se esperaría también encontrar interacciones con otras comunidades bacterianas (Nitrato reductoras, Cianobacterias, Clostridia y Metanógenas) para el acceso de donadores de electrones a partir de compuestos orgánicos fermentables (butirato, propionato y acetato)18, 19, 20. Si bien las BSR presentan un mejor desarrollo en condiciones reductoras y pH neutros, otros estudios han reportado la presencia de BSR dentro de ambientes alcalinos y condiciones oxidantes21,22 donde las bacterias adquieren un mecanismo de tolerancia fisiológica dentro de ambientes redox desfavorables desarrollando sistemas enzimáticos para la reducción y eliminación del oxigeno23.
En JK, una zona de transición, se observan mayores valores de SO-24 y Mg2+ que en PK1 y que influirían en la disminución del pH hacia valores ligeramente ácidos. Por su proximidad altitudinal a la mina, en contraste a PK se observa una reducción en la vegetación la cual esta distribuida solo alrededor de la laguna y no así en los sedimentos, aunque se observan restos de materia orgánica. La disminución de la vegetación podría deberse a la dispersión de residuos mineros contaminantes, facilitado por las condiciones climáticas de vientos fuertes y formación de oleajes.
En esta laguna, se observa la mayor distribución de BSR a lo largo del perfil sedimentario que presenta valores de Eh reductor y pH neutro con poca variación y que reflejarían condiciones óptimas para el desarrollo de cuatro (DSV, DCC, DBB, DFM) de los subgrupos de BSR observados.
Laguna Ventanani. La laguna VN ubicada a mayor altitud comprende una zona mineralizada con presencia de óxidos. Se diferencia de PK y JK por presentar menor concentración de HCO3- y por su mayor concentración de SO-24 1, así como por sus características físico-químicas de Eh oxidante y pH ácido (5 - 4.24).
Esta región además está fuertemente oxidada por su relieve escarpado, que facilitaría que el agua se mezcle con el aire influyendo sobre los valores de pH y Eh encontrados.
En esta laguna a diferencia con los sectores de MC y MG, los metales en solución no sobrepasan los límites de potabilidad para el consumo humano, en razón que la acidez no es extrema, ya que los silicatos y la precipitación de hidróxidos de hierro producirían una atenuación de la acidificación. De esta manera si el área hubiera sufrido mayor alteración se habría transformado en una fuente de drenaje ácido extremo como el de Milluni Chico colocando a descubierto los metales trazas que se encuentran combinados con los óxidos de hierro (entre estos As, Pb, Cd)1.
En VN se observó el menor porcentaje de subgrupos de BSR en los primeros 10 cm., en relación a las otras lagunas estudiadas que podría estar asociado con los elevados valores de Eh oxidante (>600 mV) a lo largo del perfil, que condicionaría un ambiente desfavorable para las BSR.
Laguna residual Milluni Chico y Lago Milluni Grande. Estas dos lagunas con características geoquímicas muy diferentes al resto de la cuenca, contienen las mayores concentraciones de SO-24 y Mg2+, así, como de metales disueltos en agua con predominancia de As>Fe>Pb>Cd>Zn>Cu>Sn, los mismos que exceden los valores permitidos por la OMS (Organización Mundial de la Salud), lo que en conjunto condicionarían la ausencia total de vegetación observada, el pH ácido y el Eh mayormente oxidante. Pese a estas condiciones se encontraron a cuatro subgrupos de BSR distribuidos en diferentes estratos del perfil. Otros estudios han reportado niveles de resistencia a elevadas concentraciones de metales pesados en las SRB24.
Así mismo la presencia de Mg2+ en forma de sales favorecería el desarrollo litotrófico de estas bacterias6.
Debido a que las aguas ácidas son deficientes en donadores de electrones25 es de esperar que en ausencia de fuentes de carbono orgánico exógeno accesible para las BSR, el hidrógeno se constituiría en principal donador de electrones, además del aporte de otras comunidades bacterianas y de la oxidación de iónes metálicos26. Las interacciones potenciales entre comunidades de bacterias hierro oxidadoras (IOB), sulfuro oxidadoras (SOB), hierro reductoras (IRB) y BSR en conjunto afectarían la movilización de metales pesados ricos en pirita27, 28, 29, 30.
MC, ubicada en la zona más contaminada, con los valores más bajos de pH, es una fuente directa de producción de drenajes ácidos. El incremento de la distribución de BSR a profundidades entre 15-33 cm. podría explicarse por la estructura de los sedimentos ácidos, con actividad de reducción de hierro dentro de la zona ácida y superficial y sulfato reducción en la parte profunda15.
MG se encuentra conectado hidrológicamente con MC, de esta forma los sedimentos contaminados son depositados en esta laguna (MG) que aunque presenta por su ubicación concentraciones de metales pesados disueltos algo menores que los encontrados en MC, éstos afectan a los valores de pH ácido observado (2). Ambas lagunas presentaron similares características (Eh oxidante y pH ácido) a nivel de los 10 cm, donde se observó un menor porcentaje de distribución de BSR, en contraste con las lagunas ubicadas cuenca arriba (PK y JK), lo que reflejaría el efecto de las condiciones físico-químicas de stress sobre el desarrollo de las BSR, asociada a los efectos de la contaminación. Es de esperar que la diversidad microbiana se encuentre también altamente reducida
Turbera Milluni TM. Si bien no se tienen datos de la distribución de metales e iones SO-24 en la turbera, su estructura constituida principalmente por material orgánico producido por la descomposición de la planta y sus características de Eh y pH, hacen suponer que aunque es un área de retención, representa una zona menos contaminada que MC y MG. La distribución de cinco subgrupos de BSR (<50-60%), entre los 20 – 40 cm. estaría directamente asociada a la concentración de materia orgánica vegetal. Esto condicionaría que las BSR dentro de ambientes a pH 6 y Eh reductor puedan desarrollarse en mejores condiciones por la disposición de sustratos orgánicos31, 12.
Las turberas se perfilarían como sistemas de bioremediacion alternativos de bajo costo, para el tratamiento de DMA y reducción de metales pesados por la accesibilidad de los microorganismos a fuentes de carbono32.
En este estudio, la actividad metabólica de BSR bajo estas condiciones proporcionadas por la turbera, favorecería el incremento de pH y la precipitación de metales provenientes de MG.
En conclusión, éste estudio demuestra la presencia de BSR en perfiles sedimentarios, de cuerpos de agua de la cuenca minera de Milluni, ante diferentes características físico-químicas, observándose una distribución espacial diferenciada de cinco subgrupos de BSR, siendo DSV-DMB, DCC-DNM-DSS los mas comúnmente encontrados en la cuenca. En las lagunas ácidas a pH 2-4, Eh oxidantes y altas concentraciones de metales pesados se encontraron a cuatro subgrupos de BSR: DSV-DMB, DCC-DNM-DSS, DBB, DFM. El subgrupo DSB fue característico de lagunas con vegetación. En conjunto estos datos demuestran la capacidad de adaptación de las BSR a diferentes ecosistemas acuáticos de stress y servirán de base a futuros estudios dirigidos a evaluar el potencial de biorremediación de estas comunidades indígenas.
AGRADECIMIENTOS
Este trabajo esta dedicado a la memoria de Marc Roulet principal impulsor de esta investigación.
Agradecemos al equipo de investigadores del IBMB, en especial al Dr. Rolando Sánchez, a Daniela Arteaga y Karina Salazar por su apoyo constante y valiosas sugerencias al trabajo.
A Matías Salvarredy por su colaboración en el trabajo de campo.
Al Programa IRD-France (HYBAM, UMR 154-LMTG, CP 9214) y Jeune Equipe SRB, por el soporte económico.
REFERENCIAS
1. Salvarredy MM, Probst A, Roulet M, Isaure MP. Contamination of surface waters by mining wastes in the Milluni Valley (Cordillera Real, Bolivia): Mineralogical and hydrological influences. Appl Geochem. 2008; 23: 1299-1324. [ Links ]
2. Apaza R. Incidencia de una contaminación por efluentes mineros sobre la fauna béntica en un complejo fluvio-lacustre alto andino. Milluni, La Paz- Bolivia. [tesis de Licenciatura]. Universidad Mayor de San Andrés: La Paz; 1991.
3. Fortin D, Roy M, Rioux JP, Thibault PJ. Occurrence of sulfate-reducing bacteria under a wide range of physico-chemical conditions in Au, and Cu-Zn mine tailings. FEMS Microb Ecol. 2002; 33: 197-208. [ Links ]
4. Luptakova A, Kusnierova M. Bioremediation of acid mine drainage contaminated by SRB. Hydrometallurgy. 2004; 77: 97-102. [ Links ]
5. Neculita CM, Zagury GJ. Biological treatment of highly contaminated acid mine drainage in batch reactors: Long-term treatment and reactive mixture characterization. J Hazard Mater. 2008; 157(2-3): 358-366. [ Links ]
6. Cao J, Zhang GJ, Mao ZS. Influence of Mg+2 on the growth and activity of sulfate reducing bacteria. Hidrometallurgy. 2009; 95: 127-134. [ Links ]
7. Hoa T T H, Liamleam W, Annachhatre AP. Lead removal through biological sulphate reduction process. Bioresour Technol. 2007; 98 (13): 2538-2548. [ Links ]
8. Medircio SN, Leão A, V, Teixeira C M. Specific growth rate of sulfate reducing bacteria in the presence of manganese and cadmium. J Hazard Mater. 2007; 143: 593- 596. [ Links ]
9. Daly K, Sharp R, McCarthy A. Development of oligonucleotide probes and PCR primers for detecting phylogenetic sub groups of sulphate-reducing bacteria. Microb Ecol. 2000; 146: 1693-1705. [ Links ]
10. Acha D, Iñiguez V, Roulet M, Guimarães JRD, Luna R, Alanoca L, Sanchez S. Sulfate-reducing bacteria in floating macrophyte rizospheres from an Amazonian floodplain lake in Bolivia and their association with Hg methylation. Appl Environ Microbiol. 2005; 71(11): 7531-7535. [ Links ]
11. Zhou J, Bruns M A, Tiedje M J. DNA recovery from soils of diverse composition. Appl Environ Microbiol. 1996; 62(2): 316-322. [ Links ]
12. Johnson DB, Hallberg KB. Acid mine drainage remediation options: a review. Sci Total Environ. 2005; 338: 3-14. [ Links ]
13. Foster AL, Munk L, Koski RA, Shanks III WC, Stillings LL. Relationships between microbial communities and environmental parameters at sites impacted by mining of volcanogenic massive sulphide deposits, Prince William Sound, Alaska. Appl Geochem. 2008; 23 (2): 279-307. [ Links ]
14. Tan GL, Shu WS, Hallberg KB, Li F, Lan CY, Huang LN. Cultivation- dependent and cultivation- independent characterization of the microbial community in acid mine drainage associated with acidic Pb/Zn mine tailings at Lechang, Guangdong, China. FEMS Microb Ecol 2007; 59: 118-126. [ Links ]
15. Kusel K. Microbial cycling of iron and sulfur in acidic coal mining lake sediments. Water Air & Soil Pollut. 2003; 3: 67-90. [ Links ]
16. Senko JM, Zhang G, Mc Donough JT, Bruns MA, Burgos WD. Metal reduction at low pH by a Desulfosporosinus species: implications for the biological treatment of acidic mine drainage. Geomicrobiol J. 2009; 26 (2): 71-82. [ Links ]
17. Geets J, Borremans B, Diels L, Springael D, Vangronsveld K, Van der Lelie D, Vanbroekhoven K. Dsr-B gene-based DGGE for community and diversity surveys of sulphate-reducing bacteria. J Microbiol Methods. 2006 Aug; 66(2):194-205. [ Links ]
18. Scheid D, Stubner S, Conrad R. Identification of rice root associated nitrate, sulphate and ferric iron reducing bacteria during root decomposition. FEMS Microb Ecol 2004; 50: 101-110. [ Links ]
19. Baumgartner LK, Reid RP, Dupraz C, Decho AW, Buckley DH., Apear JR, Przekop KM, Visscher PT. Sulfate reducing bacteria in microbial mats: Changing paradigms, new discoveries. Sediment Geol. 2006; 185: 131-145. [ Links ]
20. Briee C, Moreira D, Lopez-Garda P. Archaeal and bacterial community composition of sediment and plankton from a suboxic fresh water pond. Res Microbiol. 2007; 158(3):213-227. [ Links ]
21. OFlaherty V, Mahony T, OKenedy R, Colleran E. Effect of pH on growth kinetics and sulphide toxicity thresholds of a range of methanogenic, syntrophic and sulphate-reducing bacteria. Process Biochem. 1998; 33, 8: 555-569. [ Links ]
22. Sasaki T, Kauri T, Kudo A. Effect of pH and temperature on the sorption of Np and Pa to mixed anaerobic bacteria. Appl Radiat Isot. 2001; 55: 427-431. [ Links ]
23. Dolla A, Fournier M, Dermoun Z. Oxygen defense in sulfate reducing bacteria. J Biotechnol. 2006; 126(1):87-100. [ Links ]
24. Martins M, Faleiro ML, Barros R, Veríssimo AR, Barreiros AM, Costa CM. Characterization and activity studies of highly heavy metal resistant sulphate-reducing bacteria to be used in acid mine drainage decontamination. J Hazard. Mater. 2009; 166: 706-713. [ Links ]
25. Liamleam W, Annachhatre AP. Electron donors for biological sulphate reduccion. Biotechnol. Adv. 2007; 25: 452- 463. [ Links ]
26. Cabrera G, Pérez R, Gómez JM, Ábalos A, Cantero D. Toxic effects of dissolved heavy metals on Desulfovibrio vulgaris and Desulfovibrio sp. strains. J Hazard Mater. 2005; 135: 40-43. [ Links ]
27. 27a. Bond PL, Druschel GK, Banfield JF. Comparison of acid drainage microbial communities in physically and geochemically distinct ecosystems. Appl Environ Microbiol. 2000. 11: 4962-4971.
28. 27b. Bond PL, Smriga SP, Banfield JF. Phylogeny of microorganisms populating a thick, subaerial, predominantly lithotrophic biofilm at an extreme acid mine drainage site. Appl Environ Microbiol 2000; 66, 9: 3842-3849. [ Links ]
29. Santelli CM, Welch SA, Westrich HR, Banfield J F. The effect of Fe-oxidizing bacteria on Fe-silicate mineral dissolution. Chem. Geol 2001; 180: 99-115. [ Links ]
30. Rowe OF, Sanchez-España J, Hallberg KB, Jhonson BD. Microbial communities and geochemical dynamics in an extremely acidic, metal – rich stream at an abandoned sulphide mine (Hoelva, Spain) under pinned by two functional primary production systems. Environ Microbiol. 2007; 9(7): 1761-1771.
31. Woulds C, Ngwenya B. Geochemical processes governing the performance of a constructed wetland treating acid mine drainage, Central Scotland. Appl Geochem. 2004; 19: 1773 -1783. [ Links ]
32. Sheoran AS, Sheoran V. Heavy metal removal mechanism of acid mine drainage in wetlands: A critical review. Miner Eng. 2006; 19: 105-116. [ Links ]