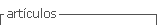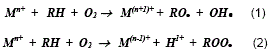Servicios Personalizados
Articulo
Indicadores
Links relacionados
 Citado por SciELO
Citado por SciELO
 Similares en SciELO
Similares en SciELO
Bookmark
Revista Tecnológica
versión impresa ISSN 1729-7532
Rev. Tecnológica v.15 n.21 La Paz jun. 2019
VINCULACIÓN TECNOLÓGICA
Antioxidantes sintéticos de matriz fenólica para conservar
comestibles con alto contenido de ácidos grasos insaturados (ÁGI)
Antioxidants synthetics of phenolic matrix, for preservation of edible,
wiht high content in unsatured fatty acids (UFA)
Erick C. Grudner Carranza*
(*), Químico Industrial, Consultor Productividad, Calidad e Innovación Tecnológica, Diplomado Investigación Operativa, Editor Revista Tecnológica, Facultad de Tecnología - UMSA.
History of the article: Received: 20/02/2019 Style review: 04/03/2019 Accepted: 02/05/2019.
Resumen
La preservación de comestibles respecto a la rancidez, es un significativo ejemplo de larga data, que demuestra cómo, los saberes empíricos y los conocimientos científicos han contribuido en la implantación de una práctica industrial, centrada en la mezcla, disolución, contacto o aspersión de la materia lipídica con sustancias naturales o compuestos químicos que manifiestan propiedades antioxidantes.
Establecida esta referencia, en el presente artículo de conocimiento y vinculación tecnológica, se exponen aspectos relacionados con: la cinética de auto-oxidación. El efecto antioxidante de cuatro compuestos fenólicos sintéticos (BHA, BHT, PG y TBHQ) capaces de interrumpir temporalmente la peroxidación. Procedimientos experimentales para determinar la estabilidad oxidativa de (AGI) periodos de inducción. Agregados sinergistas que en combinación con estos antioxidantes prolongan aun más la vida útil de comestibles lipídicos con alto contenido en (AGI), y finalmente las perspectivas futuras de sustituirlos por extractos antioxidantes fenólicos naturales, o combinarlos reduciendo así, las cantidades de uso industrial.
Palabras clave. Lípidos, Ácidos Grasos Insaturados AGI, peroxidación, rancidez, TBHQ, antioxidantes fenólicos, estabilidad oxidativa, extractos fenólicos vegetales, cinética química.
Abstract
The preservation of edible with respect to rancidity is a significant example of longstanding, which shows how empirical know and scientific knowledge have contributed to the implementation of an industrial practice, focused on mixing, dissolving, contacting or spraying the lipid material with, natural substances or chemical compounds that manifest antioxidant properties.
Established this reference, the present article of knowledge and technological link, it exposes aspects related to: the kinetics of auto-oxidation. The antioxidant effect of four synthetic phenolic compounds (BHA, BHT, PG and TBHQ) capable of temporarily interrupting peroxidation. Experimental procedures to determine the oxidative stability of (UFA) induction periods. Synergistic aggregates that, in combination with these antioxidants, further extend the shelf life of high-content (UFA) lipid comestibles, and finally the future prospects of replacing them with natural phenolic antioxidant extracts, or combine them, thus reducing the amounts of industrial use.
Keywords. Lipids, Unsaturated Fatty Acids UFA, peroxidation, rancidity, TBHQ, phenolic antioxidants, phenolic vegetable extracts, oxidative stability, chemical kinetics.
Resumo
A preservação de comestivel em relação à rancidez é um exemplo significativo de longa data, que mostra como o conhecimento empírico e científico têm contribuído para a implementação de uma prática industrial, focada na mistura, dissolução, contato ou pulverização do material lipídico com substâncias naturais ou compostos químicos que manifestam propriedades antioxidantes.
Estabelecida esta referência, o presente artigo de conhecimento e vínculo tecnológico, expòe aspectos relacionados a: a cinética da auto-oxidação. O efeito antioxidante de quatro compostos fenólicos sintéticos (BHA, BHT, PG e TBHQ) capazes de interromper temporariamente a peroxidação. Procedimentos experimentais para determinar a estabilidade oxidativa de (AGI) períodos indução. Agregados sinérgicos que, em combinação com estes antioxidantes, aumentam ainda mais o prazo de validade de compostos comestíveis lipídicos de alto conteúdo (AGI), e as perspectivas futuras de substituí-los por extratos antioxidantes fenólicos naturais ou combiná-los, reduzindo assim as quantidades de uso industrial.
Palavras-chave. Lipídeos, Ácidos Graxos Insaturados AGI, peroxidação, rancidez, TBHQ, antioxidantes fenólicos, estabilidade oxidativa, extratos vegetais fenólicos, cinética química.
INTRODUCCIÓN
Entre los constituyentes moleculares más importantes de los lípidos1, se tienen estructuras de átomos de carbono (2 a 24 en número par) formando cadenas alifáticas de grupos (-CH2-) unidas por un extremo al (-COOH grupo carboxilo), que funcionalmente caracterizan a los ácidos grasos. Dependiendo del tipo de enlaces covalentes que presente la estructura alifática (cadena), la denominación genérica común corresponderá a un: (ÁGS) Ácido Graso Saturado conformado por simples enlaces, o a un Acido Graso Insaturado (ÁGI)2 diferenciado por dobles enlaces en su estructura. [1], [2]
Varios de estos (ÁGI), no pueden ser parcial o totalmente sintetizados por el organismo humano para desarrollar determinadas funciones fisiológicas. Limitante cubierta a través de la ingesta de comestibles lipídicos y que sirven, para síntesis celulares posteriores, - ejemplo: asimilación del ácido linoleico3 C17H31COOH de las semillas vegetales para síntesis del ácido araquidónico4 C20H31COOH como precursor de estructuras moleculares eicosaniodes finales [4]-. En el cuadro 1, se representan formulaciones y grado de insaturación de algunos (ÁGI) esenciales.
Propiedades fisicoquímicas trascendentes de los ácidos grasos. Ver tabla 1.
Esta última propiedad limita la conservación natural de productos comestibles de alto contenido en (ÁGI)5, debido a la suma del oxígeno singulete6 sobre la cadena alifática, con la gravedad que una vez iniciada la auto-oxidación y al no detenerla, ésta continúa hasta deteriorar totalmente el producto (rancidez oxidativa7). [5]
En consecuencia, las procesadoras de comestibles con alto contenido (ÁGI) aplican procedimientos físicos para preservar las características de éstos, tanto en procesos de planta como en el producto final (filtrando el aire que ingresa al recinto de producción, incluyendo atmósfera de nitrógeno, envasado especial al vacío y en recipientes color ámbar) entre los más importantes. Sin embargo, cuando no es posible aplicar estos procedimientos físicos masivos y/o las condiciones económicas no lo permiten, es recomendable el uso de aditivos naturales o sintéticos (antioxidantes) para detener la auto-oxidación de (AGI), y Así, prolongar la vida útil de estos productos. [3]
Establecido este marco referencial, en el presente artículo de conocimiento y vinculación tecnológica, se considera brevemente aspectos relacionados con:
La auto-oxidación química de (AGI).
El efecto antioxidante de compuestos fenólicos primarios, utilizados para conservar comestibles con alto contenido en (AGI).
Los procedimientos experimentales para determinar la estabilidad oxidativa (periodos de inducción) de materiales lipídicos sin y con adición de antioxidantes fenólicos.
El agregado de sustancias sinergistas que añadidas junto con los antioxidantes, sirven para prolongar aun más la vida útil de comestibles lipídicos de alto contenido en AGI.
Perspectivas futuras de uso industrial.
DESARROLLO
Auto-oxidación de AGI en los lípidos
En una publicación de la revista Trans. Faraday. Society. (Farmer, E.H., Bloomfield, G.G., Sundraligam, S., y Sutton, D.A, 1942), dieron una explicación del cómo se produce la auto-oxidación8 en materiales lipídicos, estableciendo para este propósito, un mecanismo cinético de reacción con tres etapas: de iniciación, propagación y terminación .[7]
Investigaciones posteriores de: (Grosch, 1987), (Porter, y col. 1995), (Brimberg Kamal-Eldin 2003), (Frankel, 2005), (Choe y Min, 2007), (Schneider, 2009), (Hammond y White, 2011),( Barden y Decker, 2016) entre otros, establecieron que la auto-oxidación lipídica, generan peróxidos (ROOR') e hidroperóxidos (ROOH) orgánicos, a partir de reacciones en cadena involucrando radicales libres por rupturas de enlaces homolíticos en la estructura alifática del (AGI). Sitios donde el oxígeno se adicione y prosiga afectando otras estructuras lipídicas [8]. Ver cuadro 2.
Factores cinéticos que influyen sobre la auto-oxidación de AGI lipídicos, ver tabla 2.
Antioxidantes
La preservación de comestibles frente a la rancidez, es un significativo ejemplo de larga data, que demuestra cómo, los saberes empíricos y los conocimientos científicos han contribuido en la implantación de una práctica industrial, centrada en la mezcla, disolución, contacto o aspersión de la materia lipídica con sustancias naturales o compuestos químicos9 que manifiestan propiedades antioxidantes. Al respecto, los parágrafos siguientes ofrecen un compendio de eventos relacionados con este tema:
Wright, en 1852, vio como los originarios del valle de Ohio (USA) preservaban grasa de oso, usando las cáscaras del castaño de Ohio. 30 años después, fue patentado como un antioxidante. [3]
En Francia en el siglo XIX observaron que al mezclar resina de benjuí y yemas de álamo con manteca animal, se evitaba la rancidez. [3]
En el Japón investigando sobre la rancidez de los aceites de pescado, relacionaron este daño con la oxidación lipídica de triglicéridos insaturados. [3]
Émile Duclaux en 1896, planteó sobre bases experimentales que el oxígeno atmosférico, era el causante de la oxidación de ácidos grasos libres provenientes de los lípidos. [9]
Charles Dufraisse y Charles Moureu, desde 1921 y en años posteriores, iniciaron las primeras investigaciones sobre la auto-oxidación y las propiedades antioxidantes de alrededor 500 sustancias naturales y compuestos químicos, fundando un modelo investigativo experimental que se extendió por el mundo y tiene vigencia para buscar e identificar agentes que retrasen la auto-oxidación lipídica de los comestibles. [10]
Antioxidantes sintéticos fenólicos
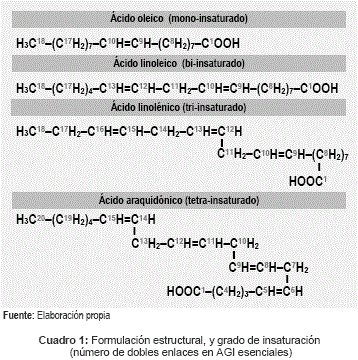
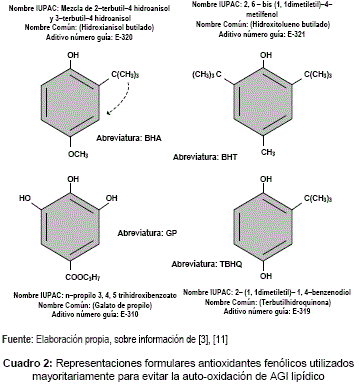
En el cuadro 2, se tienen representaciones formulares de los antioxidantes fenólicos de mayor uso industrial para extender la vida útil de los comestibles y mantener control temporal de la rancidez oxidativa de AGI lipídicos, y en la tabla 3, se describen aspectos generales de estos cuatro antioxidantes.
Comportamiento químico de antioxidantes fenólicos
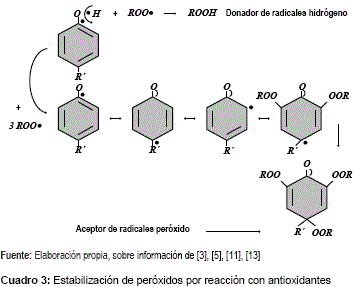
Los antioxidantes fenólicos primarios se caracterizan por detener la auto-oxidación lipídica (etapa de propagación), a través de la ruptura radicalaria de su grupo funcional y la deslocalización electrónica por resonancia en el anillo aromático conjugado. Produciendo dos reacciones:
Radicales hidrógeno para hidroperóxidar radicales peróxido,
![]()
Radicales antioxidante que reaccionan con el exceso de radicales peróxido y forman productos estables que no alteran significativamente las propiedades organolépticas y/o nutricionales de comestibles con alto contenido en AGI.
![]()
El mecanismo involucrado para impedir la propagación de radicales peróxidos por reacción y adición en la estructura del antioxidante (deslocalización por resonancia de anillo aromático conjugado), se muestra en el cuadro 3.
Antioxidantes fenólicos y estabilidad oxidativa
Descritos los aspectos cinéticos de auto-oxidación AGI, y el comportamiento antioxidante que exhiben estos cuatro compuestos fenólicos primarios, de uso frecuente y actual en la conservación de materiales lipídicos industriales con alto contenido en AGI. También es importante conocer la respuesta experimental que tienen los materiales lipídicos, frente a la estabilidad oxidativa proporcionada tanto por antioxidantes determinados (efectividad), o combinados con otros extractos vegetales y/o antioxidantes naturales10 (sinergismo).
Para medirla estabilidad oxidativa, es necesario seguir en función del tiempo la auto-oxidación del material lipídico simple (prueba de control) y acompañado por adiciones mínimas pero variable de antioxidantes en estudio. Diseño experimental que fija el período de inducción, equivalente al tiempo transcurrido para conseguir señales visibles de un consumo mayor en oxígeno, vertiginoso aumento en la concentración de peróxidos y compuestos derivados de la intensa y libre auto-oxidación. [3], [13]
Durante el periodo de inducción, la auto-oxidación AGI en su etapa de propagación se detiene, porque los radicales peróxido, reaccionan con los radicales de las estructuras antioxidantes añadidas y conforme éstas van concediendo sus centros activos, el periodo de inducción termina. En consecuencia, llegado ese momento, el material lipídico pierde la protección del antioxidante aumentando así la auto-oxidación, que se refleja en la serie de productos de reacción (análisis fisicoquímico y químico posterior) [14].
El periodo de inducción puede ser evaluado por medio de la respuesta experimental que manifiestan los materiales industriales,11 cuando éstos son expuestos a condiciones de investigación especiales que aumentan la velocidad de auto-oxidación. Al respecto, los procedimientos actuales más utilizados para medir y evaluar estabilidad oxidativa y periodos de inducción, son los siguientes:
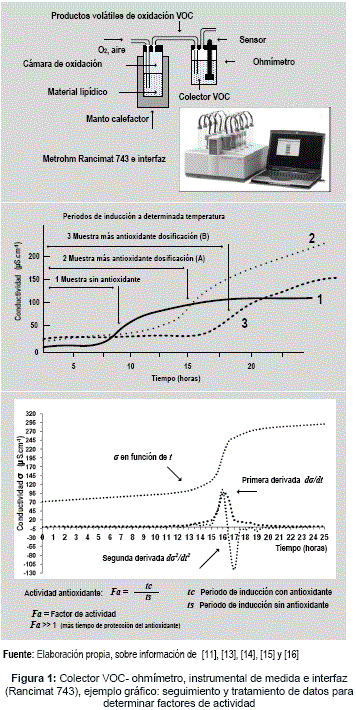
a) Ohmímetro Rancimat
Mide la estabilidad oxidativa del material lipídico, a través de una muestra que se confina en un recinto cerrado con temperatura regulable entre 50 a 220 °C, y por la cual se hace pasar oxígeno o aire a presión atmosférica. Bajo estas condiciones, la variable fisicoquímica de observación y medida corresponde al aumento en la conductividad eléctrica alcanzada, después de solubilizar los productos volátiles formados durante la auto-oxidación en el colector VOC, donde inicialmente se tiene un de volumen líquido específico con baja conductividad (agua desionizada).
La conductividad es registrada y graficada continuamente para obtener series temporales (conductividad-tiempo) ascendentes, caracterizadas por puntos de inflexión que señalan la finalización de los periodos de inducción, y es a partir de este punto, que se incrementa la conductividad eléctrica del colector VOC, indicando la desprotección del material lipídico. En la figura 1, se muestra un esquema básico del colector de productos volátiles VOC -ohmímetro y su desarrollo para medidas automáticas con opción de interfaz, como lo hace el equipo (Metrohm Rancimat 743), A más de un modelo gráfico (seguimiento y tratamiento de datos) para determinar los periodos de inducción.
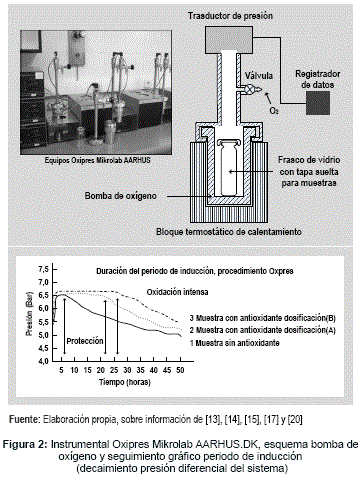
b) Oxidación a presión alta OXIPRES
Por este procedimiento se logra oxidar rápidamente una muestra de material lipídico al introducirlo en el frasco de vidrio, contenido en la cámara hermética y suministrar oxígeno a presión (>5 bar = 4,935 atm), fijando además la temperatura de los ensayos entre 90 a 120°C. Estado inicial de condiciones que se aprovecha para medir y registrar variaciones de presión, originadas por consumo de oxígeno durante la auto-oxidación.
Por lo que la cámara hermética (bomba de oxígeno) en unión con el transductor de presión12 detecta los cambios en la atmósfera interior, y envía estas señales a un grabador que las convierte y grafica en series temporales de (presión-tiempo), marcando tres sectores: 1) Ascenso proporcional de presión con el aumento de temperatura, 2) estabilidad de la presión final, y 3) caída brusca de presión, relacionada con la desprotección del material lipídico frente a la acción del oxígeno. La figura 3, muestra tres equipos Oxipres Mikrolabm AARHUS.DK para muestras simultáneas, la bomba de oxígeno a alta presión y temperatura de ensayo, más el rastreo gráfico para fijar los periodos de inducción, en función de la caída de presión diferencial en el sistema.
Agregados sinergísta13
No presentan acción antioxidante específica, no obstante, su añadido tiene la capacidad de aumentar la efectividad del antioxidante primario14. El comportamiento se explica a través de los dos mecanismos siguientes:
1) Antioxidante primario AxH y agregado sinergista AsH, ambos con afinidad química diferente por radicales peróxido
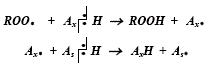
AsH reacciona lentamente con radicales peróxido, en especial por impedimento estérico. Así, los radicales antioxidante Ax, pueden reaccionar con AsH para regenerar AxH. [11]
2) Acción combinada aceptor de radicales peróxido AxH y un QHq secuestrador de metales :
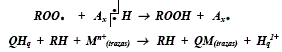
Aportando al medio ácido para la estabilidad de los antioxidantes fenólicos, e inhibiendo la acción catalítica de iones metálicos (Cu y Fe) sobre la peroxidación lipídica, (ecs.1 y 2). [11]
En la tabla 4, se dan a conocer algunos pares frecuentes de uso industrial: antioxidante fenólico primario - agregado sinergísta.
Uso de antioxidantes BHA, BHT, PG y TBHQ
Si bien, el procedimiento vigente de aplicación industrial de antioxidantes fenólicos sintéticos desde hace 79 años, establece que son inofensivos para el consumo humano, siempre y cuando las cantidades de antioxidantes en los comestibles se mantengan por debajo de las tolerancias permitidas. Pruebas de laboratorio usando como variable de observación la ingesta de comestibles procesados con estos antioxidantes por especies animales menores, les atribuyen el desarrollo de procesos descontrolados en la división de las células del cuerpo (cáncer) [18], [19]. Resultado que está sirviendo de alerta para investigar con sustitutos naturales o mezclas combinadas que permitan reducir las cantidades límites de adición, o descarten los usos futuros de los antioxidantes fenólicos sintéticos.
La apertura de este nuevo campo de investigación sobre auto-oxidación de materiales lipídicos, incluye pruebas de estabilidad oxidativa, incorporando extractos vegetales de composición fenólica15 simple y compleja con potenciales propiedades antioxidantes. [3]
CONCLUSIONES
Por todo lo expuesto, se puede compendiar el estado de arte a partir del conocimiento fisicoquímico y aplicación industrial de antioxidantes fenólicos frente a la oxidación lipídica (rancidez), de la siguiente manera:
Se conoce que el origen de la rancidez lipídica se debe al oxígeno atmosférico, y la peroxidación radicalaria generada se descompone principalmente en productos de primera generación: (dienos conjugados, aldehídos) que después desarrollan a dialdehídos, y compuestos cíclicos.
Es posible controlar temporalmente la oxidación, usando los antioxidantes fenólicos sintéticos: E-320 (BHA), E-310(GP), E-321 (BHT) y E-319 (TBHQ), en las dosificaciones másicas límite permitidas (tolerancias de adición).
Se conoce cómo el antioxidante de matriz fenólica natural o sintético, protege el material lipídico frente a la peroxidación.
Se puede experimentar y controlar la cinética de oxidación lipídica, aplicando procedimientos experimentales (rancimat y oxipres), que evalúan la estabilidad oxidativa del material lipídico en función de la temperatura (procesos de inducción o tiempo de preservación del antioxidante), y en función a sus resultados, fijar tiempos de vida útil en almacenamiento de comestibles lipídicos con alto contenido en AGI.
Aún manteniendo su vigencia por un largo tiempo (79 años) y teniendo aprobación de uso general por no afectar la salud humana, se anticipa razonadamente que pueden dañar a ésta [18]. Motivo de alerta que ha originado abrir un nuevo campo de investigación, que busca respuesta experimental en relación al agregado de extractos vegetales de matriz fenólica simple o compleja (antes no tomados en cuenta) y su efecto en los materiales lipídicos (estabilidad oxidativa, tiempo de vida útil del comestible). Reportando importante información que aun siendo particular para materiales lipídicos determinados, no excluye su contribución en un procedimiento innovador que utilice antioxidantes naturales, reduciendo así, el actual uso de estos cuatro antioxidantes fenólicos sintéticos en las procesadoras de comestibles lipídicos con alto contenido en AGI. [3]
NOTAS
1 Biomoléculas constituidas mayoritariamente por carbono e hidrógeno, oxígeno en menor proporción y elementos traza (fósforo, azufre y nitrógeno). Debido a su estructura, son moléculas hidrófobas (insolubles en agua). Los lípidos (triacilglicéridos, ácidos grasos, fosfolípidos y esteroles) se encuentran en la mayoría de los materiales biológicos que se consumen como alimentos y/o se agregan como ingredientes funcionales en muchos alimentos procesados, aportando cualidades de textura, estructura, palatividad y color. [3]
Sin embargo, los lípidos de los alimentos son químicamente inestables y susceptibles a reacciones en cadena de radicales libres que no solo deterioran los comestibles lipídicos sino que también producen fragmentos oxidados, siendo algunos volátiles que se perciben desprendiendo olores y sabores de rancidez, además de entrecruzar los lípidos y otras macromoléculas en polímeros no nutritivos. [2]
2 Aceites comestibles de diferentes vegetales y semillas, leche y sus derivados, cacao, pescados, carnes avícola, porcina, y comestibles procesados que incluyen lípidos.
3 IUPAC Ácido (9Z, 12Z) -9,12- octadecadienoico.
4 IUPAC Ácido(5Z, 8Z, 11Z, 14Z)-5,8, 11, 14-eicosatretaenoico.
5 Aceites comestibles de diferentes vegetales y semillas, leche y sus derivados, cacao, pescados, carnes avícola, porcina, y comestibles procesados que incluyen lípidos.
6 El oxígeno molecular singlete, es una especie activada y reacciona especialmente con los dobles enlaces (reacciones de adición). Su química es diferente a la del oxígeno triplete. [6]
7 Degradación de los AGI, y formación de peróxidos o hidro-peróxidos que posteriormente se polimerizan y descomponen en aldehídos, cetonas y ácidos de menor peso molecular influyen sobre el sabor y olor, además de producir la alteración de las vitaminas liposulubles A, y E. [3]
8 Reacción iniciada por el oxígeno (agente oxidante) sobre los AGI lipídicos.
9 Del extenso grupo de agentes inhibidores de la auto-oxidación lipídica, sólo algunos son aptos para consumo humano, por lo que en su selección es necesario tener en cuenta lo siguiente [11]:
• La eficacia de cantidades muy pequeñas (0,001 a 0,01%),
• Ausencia de cambios en el color, olor, sabor y otras características del comestible,
• Compatibilidad con el comestible y su fácil aplicación,
• Estabilidad en las condiciones del proceso y almacenamiento,
• El compuesto y sus productos de oxidación no pueden ser tóxicos, aún, si la dosis es mucho mayor a la que normalmente se ingiere en el comestible.
• Otros factores: legislación, costo, preferencia por antioxidantes naturales.
10 Principalmente tocoferoles, flavonoides, xantofilas y caroteniodes.
11 Comestible provisto de material lipídico y el o los respectivo(s) antioxidante(s).
12 Sensor de presión de gases o líquidos que genera una señal (neumática o eléctrica) diferente en función de la presión a la cual está sometido.
13 Perteneciente o relativo a la sinergia: Acción de dos o más causas que producen un mayor efecto al que se produce por adición de los efectos individuales.
14 Sin embargo, combinaciones adecuadas de antioxidantes primarios pueden también manifestar un comportamiento sinérgico. El caso más importante es la combinación de BHA y BHT en la conservación de procesados de cacao (chocolates). [3]
15 Destacando por ejemplo los extractos de: oregano (timol), romero (carnosol), salvia (ácido carnósico), carotenoides (vitamina A), perejil (flavonoides), argán (derivados cinámico - ácido cafeico), sésamo, espárragos (alfa tocoferoles componentes principales de la vitamina E). Según la importante información académica (publicaciones) que viene reportando este nuevo campo de investigación. [3], [8]
BIBLIOGRAFÍA
[1] Koolman, J., Röhm, H.K., 2005, Bioquímica texto y atlas, Lípidos, pp: 46-48, Ed. Panamericana Médica, 3era edición, Madrid-España, [ Links ]
[2] Berg, M, J., Tymoczko, L.J., Stryer, L, 2008 bioquímica, versión en español, Capítulo 12 Lípidos y membranas celulares, pp: 326-320, ISBN: 978842917006-1, Barcelona-España, [ Links ]
[3] Ramalho, V., Neuza, J., 2005, Antioxidantes utilizados em óleos, gorduras e alimentos gordurosos, Quim. Nova, Vol. 29, No. 4, 755-760, 2006, Socidade Brasileira de Química, Brasil- São José do Rio Preto - SP, Recuperado de: quimicanova.sbq.org.br/default.asp?ed=83, [ Links ]
[4] Ácido araquidónico, origen, propiedades, usos y funciones, https://acidos.info> araquidónico, consulta: 10/02/2019,
[5] Castañeda, M., Deterioro de lípidos, auto-oxidación, Recuperado de: depa.fquim.unam.mx/amyd/archivero/2Lipidos-2_24644.pdf, [ Links ]
[6] Recuperadonde: https://es.wikip.org/w/index.php?title=Oxígeno_triplete&oldid=10102339»3
[7] Mechanism of the reactions of oxygen with fatty materials. Advances... https://link.springer.com/article/10.1007/BF02645889DeSaussure, Ann. chim. et Phys. [2]13, 337... Farmer, E. H., Bloomfield, G. F., Sundralingam, A., and Sutton, D. A., Trans.... George, P., and co-workers, Nature149, 601 (1942); Trans. Faraday Soc.42, 210 and 217 (1946); Proc. Roy. Soc.,
[8] García, M. MC., 2018, oxidación lipídica en productos lácteos: influencia de la adición de ácidos grasos funcionales, Tesis, p: 18, Universidad Autónoma de Madrid, Instituto de Ciencia y Tecnología de Alimentos y Nutrición (CSIC), España, [ Links ]
[9] https://es.wikip.org>wiki>Émile, Consulta 21/02/2019,
[10] Citados por Meurant, G., 2012, Atmospheric oxidation and antioxidants, p:5, https://books google.com.bo> books, Consulta 21/02/2019, [ Links ]
[11] Antioxidantes - depa.fquim.unam.mxdepa.fquim.unam.mx/amyd/archivero/8-Lipidos6_26590.pdf
[12] CODEX STAN 192-1995, Ggeneral standard for food additives, Recuperado de: www.fao.org/gsfaonline/docs/CXS_192e.pdf [ Links ]
[13] Castañeta, M., Peroxidación de lípidos - depa.fquim.unam.mx Recuperado de: depa.fquim.unam.mx/amyd/archivero/lipidos-4_24710.pdf, [ Links ]
[14] Andrade, A. P., 2017, Metodología novedosa para la evaluación del tiempo de vida de alimentos con alto contenido en grasa, Recuperado de: lacongress.aocs.org/.../Presentations/Andrade.pdf, [ Links ]
[15] Carné, S., Estévez, J., Evaluación de la oxidación y la protección antioxidante en materias primas & pienso, Recuperado de: www.itpsa.com/images/stories/pdfs/antioxidantes, [ Links ]
[16] www.metrohm.com/.../stability-measurement/rancimat
[17] Mmikrolab.dk/amfile/file/download/file_id/131817/- Højbjerg - Denmark
[18] www.portalantioxidantes.com/faq/ ¿Existe riesgos asociados al consumo crónico de antioxidantes sintéticos?, Consulta: 23/02/2019,
[19] IARC -I nternational Agency for Research on Cancer, www.iarc.fr
[20] Prime, D., antioxidants- fish meal and feed, april 2018 Recuperado de: sfs.is>Antioxidants-Vitablend-Dvid-Prime, pdf. [ Links ]